Puntos clave
- La obesidad se caracteriza por un exceso de tejido adiposo disfuncional, lo que provoca inflamación crónica de bajo grado, resistencia a la insulina y síndrome cardiometabólico relacionado con la obesidad, afectando a múltiples órganos y aumentando el riesgo cardiovascular.
- La pérdida de peso, incluso en una cantidad moderada, puede mejorar de manera significativa los factores de riesgo cardiometabólico, y una mayor pérdida de peso se relaciona con beneficios más importantes para la salud, incluidas reducciones en las tasas de mortalidad y morbilidad.
- Los nuevos medicamentos contra la obesidad, en particular los agonistas del receptor GLP-1, representan un avance importante en el tratamiento de la obesidad, ya que ofrecen el potencial de lograr una pérdida de peso considerable y mejores resultados de salud, aunque factores como el costo y la adherencia al tratamiento siguen siendo consideraciones clave.
Este artículo analiza la obesidad como una condición caracterizada por un exceso de tejido adiposo disfuncional, que contribuye a la inflamación crónica de bajo grado, la resistencia a la insulina y el síndrome cardiometabólico asociado a la obesidad. Examina los beneficios de la pérdida de peso, las limitaciones de las intervenciones de estilo de vida y la aparición de medicamentos contra la obesidad como el nuevo estándar de atención.
La obesidad se ha convertido en una epidemia global, con tasas que se han más que triplicado entre 1975 y 2022.¹ Según la World Obesity Federation, casi 3,000 millones de personas se clasifican actualmente como con sobrepeso u obesidad, lo que impulsa aumentos globales en morbilidad y mortalidad. Para comprender por qué importa el tratamiento, es fundamental analizar la biología de la obesidad y sus efectos sistémicos.
La biología de la obesidad
El cuerpo contiene dos principales depósitos de grasa: el tejido adiposo subcutáneo (SAT), que es la grasa almacenada justo debajo de la piel, y el tejido adiposo visceral (VAT), que se acumula más profundamente en el abdomen, rodeando los órganos internos. Con el aumento de peso, es principalmente el VAT el que se expande, a través de la hipertrofia de los adipocitos, más que el SAT.
Dado que la grasa no puede redistribuirse del VAT al SAT, una vez que el VAT alcanza su límite de almacenamiento, el exceso de grasa empieza a acumularse en órganos y tejidos que normalmente son magros.
Este proceso, conocido como depósito de grasa ectópica, afecta al corazón, hígado, riñones, músculos y páncreas, y provoca lipotoxicidad en estos órganos. La magnitud del depósito ectópico de grasa se correlaciona con el grado de adiposidad visceral.²
El tejido adiposo es una glándula activa con funciones endocrinas y metabólicas. Los adipocitos, o células grasas, secretan al menos 600 adipocinas diferentes: un conjunto de hormonas, péptidos bioactivos y proteínas.³
En condiciones normales, las adipocinas ayudan a mantener el equilibrio entre señales antiinflamatorias y sensibilizadoras de la insulina (p. ej., adiponectina, omentina) y señales proinflamatorias y resistentes a la insulina (p. ej., leptina, TNF-alfa, IL-6). Cuando se desarrolla obesidad, especialmente debido a la expansión de los adipocitos viscerales, este equilibrio se desplaza. El resultado es inflamación crónica de bajo grado y resistencia a la insulina, que derivan en disfunción endotelial y síndrome cardiometabólico relacionado con la obesidad.³
Más allá del daño causado por la acumulación ectópica de lípidos (lipotoxicidad), los propios depósitos de grasa ectópica secretan adipocinas inflamatorias adicionales, lo que contribuye a lesiones locales en los órganos y a un aumento del riesgo cardiovascular.⁴ Un ejemplo es la grasa epicárdica, ubicada en el espacio pericárdico y dentro del miocardio, que actúa tanto como marcador de riesgo cardiovascular como precursor de patología cardíaca. Como ejemplo concreto, puede representar un factor de riesgo independiente para el desarrollo de fibrilación auricular.⁵
De manera similar, la grasa visceral intrahepática, ubicada dentro y alrededor de los hepatocitos, puede conducir a la enfermedad hepática esteatósica asociada a disfunción metabólica (MASLD). Esta puede progresar a esteatohepatitis asociada a disfunción metabólica (MASH) y, en última instancia, a fibrosis (es decir, cirrosis). La MASLD no solo representa un riesgo conocido de enfermedad hepática, sino que también actúa como factor de riesgo independiente para la enfermedad cardíaca aterosclerótica.⁶
El síndrome cardiometabólico relacionado con la obesidad (CMS), denominado por la American Heart Association como síndrome cardiovascular-renal-metabólico (CKM), se define como «un trastorno sistémico caracterizado por interacciones fisiopatológicas entre los factores de riesgo metabólicos, la enfermedad renal crónica (CKD) y el sistema cardiovascular, que derivan en disfunción multiorgánica y una alta tasa de eventos cardiovasculares adversos».⁷
Esta condición está impulsada por la acumulación de exceso de tejido adiposo disfuncional, que provoca inflamación, estrés oxidativo y resistencia a la insulina.
Desde la perspectiva del seguro, el impacto más relevante del CMS es su fuerte asociación con la morbilidad y mortalidad cardiovascular.
La frase «trastorno sistémico que conduce a disfunción multiorgánica» resalta las amplias consecuencias del CMS, incluido el desarrollo de hipertensión, dislipidemia, hiperuricemia y prediabetes, condición que suele acompañarse de glucotoxicidad y posible progresión a diabetes mellitus tipo 2 (DM2).
Además de estos efectos metabólicos centrales, el CMS contribuye a una amplia gama de otras afecciones, entre ellas enfermedades respiratorias, demencia, apnea obstructiva del sueño y una mayor incidencia de cánceres relacionados con la obesidad.
Beneficios de la pérdida de peso en mortalidad y morbilidad
El tratamiento eficaz del síndrome cardiometabólico relacionado con la obesidad (CMS) debe incluir idealmente dos componentes:
- Abordar la causa subyacente: el sobrepeso y la obesidad.
- Tratar las complicaciones, como la hipertensión, la dislipidemia o la diabetes tipo 2.
Hasta hace poco, no existían terapias ampliamente disponibles que trataran eficazmente la obesidad en sí. Como resultado, el tratamiento se centraba en los factores de riesgo asociados sin reducir la grasa visceral o ectópica que impulsa la enfermedad. Este enfoque dejaba a las personas con un riesgo persistentemente elevado de mortalidad y morbilidad.
¿La pérdida de peso reduce los adipocitos disfuncionales en el VAT y en los depósitos ectópicos, y mejora el riesgo cardiometabólico?
La respuesta corta es sí.
Con la pérdida de peso, se produce una reducción preferencial de la grasa visceral. Un estudio mostró que pérdidas del 5%, 11% y 16% se asociaron con disminuciones respectivas del 9%, 23% y 30% en la grasa intra abdominal (medida en cm³). Aún más significativas fueron las reducciones en triglicéridos intrahepáticos ectópicos de 13%, 52% y 65%, respectivamente, medidas por resonancia magnética.⁸
Los factores de riesgo cardiometabólico comienzan a mejorar incluso con una pérdida de peso modesta, con una mayor mejoría a medida que se pierde más peso. Una reducción del 5% conduce a una mejora significativa en la sensibilidad a la insulina tanto en el hígado como en el tejido adiposo, mientras que una pérdida mayor del 11%-16% es necesaria para mejorar significativamente la sensibilidad a la insulina en el músculo. Los marcadores inflamatorios no tienden a mejorar con una pérdida del 5%, pero sí muestran reducciones significativas con una pérdida del 11%-16%.⁸
Estos efectos se observan clínicamente. Una reducción del 2%-5% del peso mejora la glucosa en ayunas y la HbA1c en la diabetes tipo 2. En personas con intolerancia a la glucosa, cada kilogramo perdido reduce en un 16% el riesgo de progresión a diabetes tipo 2. Una pérdida del 2%-5% también mejora los triglicéridos y la presión arterial sistólica, pero se requiere una pérdida del 5%-10% para mejorar el colesterol HDL y reducir la presión arterial diastólica.
Una pérdida del 5%-10% también se asocia con una reducción del dolor y una mejor función en personas con osteoartritis, una disminución de la grasa hepática en quienes tienen MASLD y una desaceleración del deterioro de la movilidad relacionado con la edad. Estos beneficios se han observado en la mayoría de los programas de modificación del estilo de vida, que típicamente logran pérdidas del 3%-7% sin medicación.⁹
Una pérdida de peso mayor, del 10%-20%, suele requerir el uso de los nuevos medicamentos contra la obesidad, como semaglutida (Wegovy, un agonista del receptor GLP-1 – glucagon-like peptide-1 receptor agonist) o tirzepatida (Zepbound, un agonista dual de GLP-1 y GIP – glucose-dependent insulinotropic polypeptide). Con este nivel de reducción ponderal, los estudios han mostrado mejoría en las puntuaciones de MASH (basadas en biopsia hepática) y en el índice de apnea-hipopnea (AHI) en personas con apnea obstructiva del sueño.¹⁰
Pérdidas de peso superiores al 20% se habían observado, hasta hace poco, principalmente en personas sometidas a cirugía bariátrica. Una revisión sistemática y metaanálisis encontró que, en comparación con los controles, la cirugía bariátrica se asociaba con:
Figura 1:¹¹ Primer metaanálisis
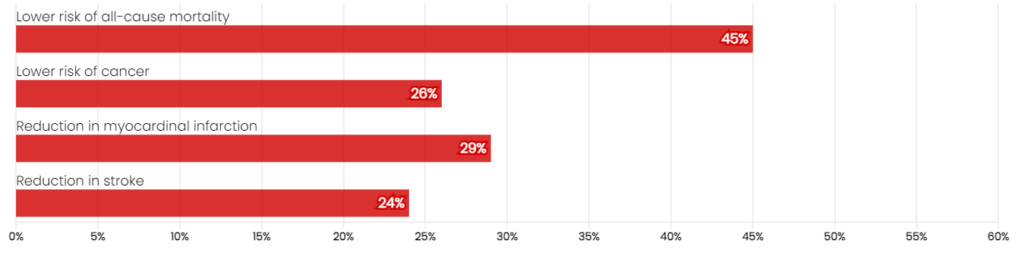
Un metaanálisis independiente que comparó la cirugía bariátrica con los controles informó reducciones igualmente significativas:
Figura 2:¹² Segundo metaanálisis
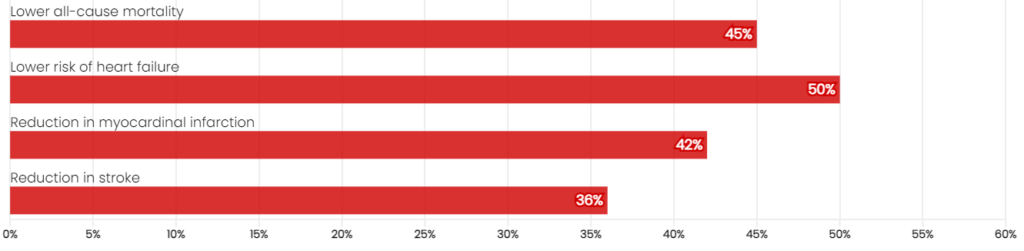
Estos hallazgos se basan en estudios controlados no aleatorizados y están a la espera de confirmación en ensayos clínicos aleatorizados.
El efecto GLP-1
Se ha observado una pérdida de peso superior al 20% en:
Figura 3: Pérdida de peso superior al 20%
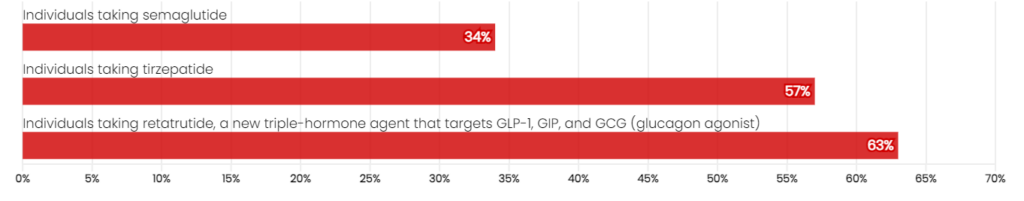
Una pérdida de peso superior al 25% no se ha observado con semaglutida, pero sí ocurre en:
Figura 4: Pérdida de peso superior al 25%
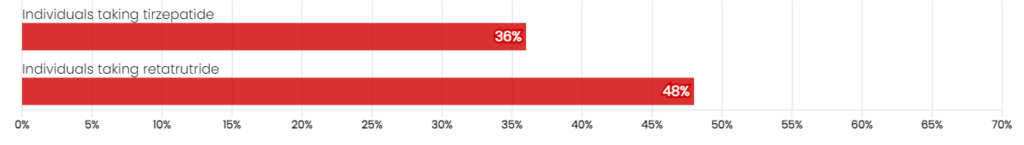
Una pérdida de peso superior al 30% solo se ha observado en estudios con retatrutida, que afectó al 26% de los pacientes. Este medicamento se encuentra actualmente en desarrollo, con un lanzamiento previsto por Eli Lilly para 2027.¹³,¹⁴,¹⁵
RGA ha analizado el impacto de estos medicamentos en la mortalidad y la morbilidad a nivel poblacional.
Las formulaciones orales de semaglutida (es decir, 50 mg/día) y un agonista no peptídico del receptor GLP-1 (GLP-1RA) llamado orforglipron podrían reducir los costos y mejorar el acceso una vez aprobados.
Otro aspecto a considerar es la interrupción del tratamiento. Cuando se suspenden los medicamentos GLP-1, el peso perdido suele recuperarse. En cambio, su uso continuado ha demostrado mantener la pérdida de peso durante hasta cuatro años.¹⁶
Desde el punto de vista médico, no sorprende que dejar de usar GLP-1RAs genere con frecuencia recuperación del peso: del mismo modo que suspender medicamentos antihipertensivos o antidiabéticos puede hacer que la presión arterial o la glucosa vuelvan a elevarse.
En estudios de uno y dos años, las tasas de discontinuación de los GLP-1RAs fueron:
- El 47% y el 64% en personas con diabetes tipo 2.
- El 65% y el 84% en personas sin diabetes tipo 2.
Las tasas más bajas de discontinuación se asociaron con una mayor pérdida de peso, ingresos más altos y menos efectos gastrointestinales. Cuando se recuperaba el peso tras suspender el tratamiento, los pacientes con frecuencia reiniciaban la terapia. Las tasas de reinicio al año y a los dos años fueron:
- El 47% y el 57% en quienes tenían diabetes tipo 2.
- El 36% y el 46% en quienes no tenían diabetes tipo 2.¹⁷
La estrategia óptima para el mantenimiento del peso a largo plazo, ya sea con dosificación continua, microdosificación o uso intermitente, sigue siendo incierta y requiere futuras investigaciones.
Aspectos destacados de la investigación de RGA
Mortalidad poblacional
- Para 2045, los medicamentos basados en incretinas, como los GLP-1, podrían reducir la mortalidad en EE. UU. en un 3,5% en un escenario central, un 8,8% en uno optimista y un 1,0% en uno pesimista.
- En el mismo escenario central, la mortalidad podría disminuir un 2,0% en el Reino Unido, un 2,6% en Canadá y un 1,4% en Hong Kong.
- Las mejoras en mortalidad variarán según la edad, con reducciones mayores entre los 45 y 59 años y menores a partir de los 85 años.
Morbilidad poblacional
- Las poblaciones podrían ver reducciones más pequeñas, pero aun así positivas, en la incidencia de cánceres durante el mismo periodo.
Mortalidad y morbilidad asegurada
- Los grupos asegurados y los rentistas probablemente experimenten reducciones algo menores en mortalidad y morbilidad que la población general.
Conclusión: el camino a seguir
Los nuevos medicamentos antiobesidad basados en GLP-1 representan un avance significativo en el tratamiento de la causa subyacente del síndrome cardiometabólico relacionado con la obesidad. Al actuar directamente sobre la disfunción del tejido adiposo, estas terapias tienen el potencial de reducir la morbilidad y la mortalidad asociadas con la obesidad.
Para las aseguradoras, factores como el acceso, la adherencia y los resultados a largo plazo harán que el impacto en el seguro sea más matizado. Además, la evaluación precisa del riesgo en personas que utilizan estas nuevas terapias con GLP-1 requerirá un análisis especializado por parte del área de suscripción.