Consideraciones Clave
- El H5N1 —también conocido como gripe aviar o influenza aviar— no es un virus nuevo. Fue identificado por primera vez en 1996 y, desde entonces, se ha propagado entre aves silvestres en todo el mundo.
- Las personas que han estado previamente infectadas con otros subtipos de influenza A (como el H1N1) o que han sido vacunadas contra ellos, podrían beneficiarse de una inmunidad cruzada frente al H5N1.
- Dado que no existe evidencia, hasta la fecha, de una transmisión sostenida de persona a persona, el riesgo actual de una pandemia por H5N1 sigue siendo bajo.
A comienzos de 2025, un hombre en Luisiana falleció tras haber sido hospitalizado con un cuadro grave de gripe aviar. Su fallecimiento, ocurrido a principios de enero, desató una serie de reportajes en los medios que abordaban los posibles peligros del virus H5N1.¹
Hasta el 18 de marzo, se han confirmado 70 casos de infección humana este año por lo que, comúnmente, es un virus de origen animal.² De esos 70 casos, solo el del hombre en Luisiana ha sido fatal.
¿Cuál es exactamente la amenaza que representa el virus H5N1? ¿Qué tan probable es que enfrentemos otra pandemia global tan pronto después del surgimiento del COVID-19?
Este artículo analiza la historia del H5N1, la naturaleza del virus y los posibles peligros que podría representar.
Dentro del virus
El H5N1 —también conocido como gripe aviar o influenza aviar— no es un virus nuevo. Fue detectado por primera vez en 1996 en China. Al año siguiente, se propagó rápidamente entre las aves de corral en Hong Kong. Tras 18 infecciones humanas, ninguna de ellas mortal, su propagación se desaceleró.
El virus resurgió en 2003, con brotes significativos en aves en toda Asia, y posteriormente en África y Europa. Se registraron infecciones humanas esporádicas. En 2022, el virus mutó y surgió un nuevo subtipo de H5N1. Esta versión era genéticamente diferente de las variantes anteriores y se propagó a América del Norte, infectando tanto aves de corral domesticadas como especies de mamíferos silvestres. En el último año, este nuevo subtipo también ha comenzado a propagarse entre vacas lecheras.
Esta versión del virus está diezmando las poblaciones de aves. Funcionarios de salud de las Naciones Unidas estiman que ha causado la muerte de más de 300 millones de aves en todo el mundo. Hasta marzo de 2025, más de 166 millones de aves habían sido infectadas en Estados Unidos, y su propagación a vacas lecheras representa un fenómeno tanto nuevo como inesperado.
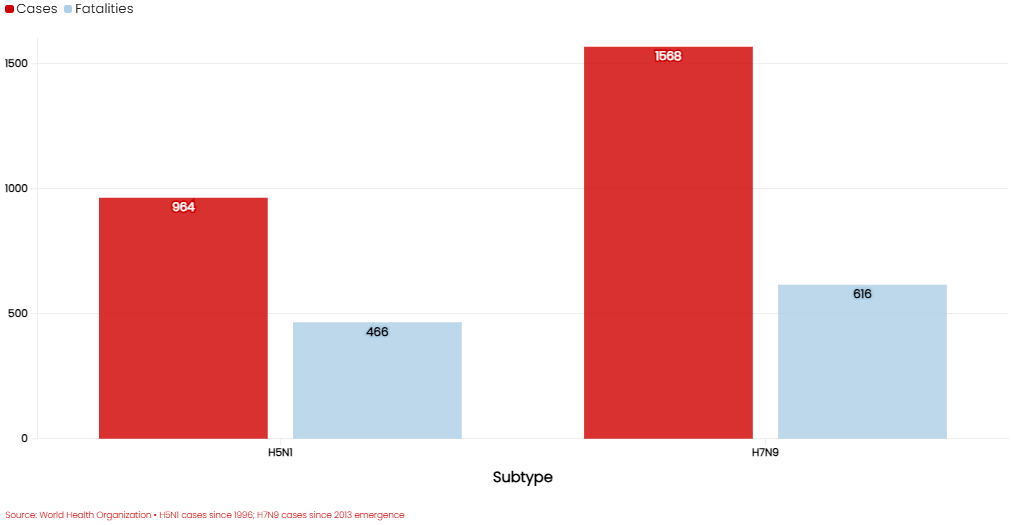
Desde su aparición en 1996, se han reportado 964 casos confirmados en laboratorio de H5N1 en humanos en 24 países, de los cuales 466 —es decir, el 48 %— resultaron fatales. Una variante distinta, el H7N9, ha infectado a 1,568 personas desde 2013, con 616 muertes reportadas (39 %), según datos de la Organización Mundial de la Salud (OMS).
Sin embargo, es mucho más probable que se reporten los casos graves que los leves, por lo que se estima que la tasa real de infección/mortalidad es considerablemente más baja.
Infecciones y muertes por gripe aviar a nivel mundial
El hombre de Luisiana que falleció a causa del H5N1 a principios de 2025 tenía más de 65 años y, según se informó, padecía afecciones médicas preexistentes. Fue hospitalizado tras haber estado expuesto a un grupo de aves de traspatio y a aves silvestres.
La infección por H5N1 en humanos presenta una amplia variedad de manifestaciones clínicas. Algunos pacientes permanecen asintomáticos, mientras que otros desarrollan un abanico de síntomas, que van desde conjuntivitis y afecciones leves del tracto respiratorio superior hasta enfermedades del tracto respiratorio inferior, como neumonía —e incluso la muerte.
Cuarenta y seis personas en Estados Unidos contrajeron H5N1 entre marzo y octubre de 2024. Todos presentaron síntomas leves con una duración media de solo cuatro días, y ninguno fue hospitalizado ni falleció. La detección temprana y el tratamiento antiviral oportuno podrían haber contribuido a estos resultados favorables.
Además, no se identificaron casos humanos adicionales entre los contactos cercanos de las personas que dieron positivo al virus, lo cual es coherente con la falta actual de evidencia sobre la transmisión de persona a persona del H5N1 en Estados Unidos.³
Un estudio publicado en 2016, que analizó casi dos décadas de infecciones graves causadas por dos subtipos de gripe aviar —H5N1 y H7N9—, concluyó que las personas tienden a desarrollar la inmunidad más fuerte frente a los virus de la influenza durante la infancia, lo que podría brindar una protección de por vida. Ese estudio mostró que la inmunidad adquirida tras una primera infección ofrecía un 75 % de protección contra enfermedad grave y un 80 % contra la muerte, siempre que se tratara de un virus de gripe aviar coincidente.⁴ ⁵
Una investigación publicada en 2025 en Nature Medicine encontró que el año de nacimiento de una persona estaba estrechamente relacionado con la cantidad de anticuerpos contra el H5N1 presentes en su sangre. Los adultos mayores nacidos antes de 1968, que estuvieron expuestos en su infancia a virus estacionales de influenza H1N1 o H2N2, parecían tener respuestas inmunitarias que perduran toda la vida. Si bien estos anticuerpos con reactividad cruzada probablemente no previenen las infecciones por H5N1, se cree que podrían reducir la gravedad de la enfermedad.
¿Riesgo de una nueva pandemia?
A comienzos de 2025, el riesgo actual de que el virus H5N1 genere una pandemia humana grave sigue siendo bajo. Por el momento, la transmisión de persona a persona parece ser extremadamente limitada o incluso inexistente. Con excepción de un caso en el que no se pudo determinar la fuente de exposición, todos los demás pacientes habían tenido contacto laboral con animales infectados.
Dicho esto, la vigilancia continua de este virus es esencial para comprender cómo está evolucionando.
Aunque la mayoría de los patógenos de origen animal no se adaptan fácilmente al ser humano, el virus H5N1 ha mostrado una actividad sostenida —e incluso creciente— en su capacidad para infectar animales silvestres y domésticos, y ha mutado para propagarse a nuevas especies. Cada vez que el virus se adapta a un nuevo hospedador mamífero, adquiere nuevas características y da un paso más hacia una posible transmisión más eficaz entre humanos. De hecho, la mayoría de las pandemias modernas se han originado por la transmisión de patógenos zoonóticos entre animales y personas. Por ejemplo:
La pandemia de gripe porcina de 2009 (H1N1/09) causó unas 575,000 muertes y pareció ser una nueva cepa de H1N1, resultado de una triple recombinación de virus de gripe aviar, porcina y humana.
La pandemia de gripe española (H1N1), que provocó hasta 100 millones de muertes, surgió en 1918 a partir de aves silvestres.
La gripe asiática (H2N2) causó hasta 1.5 millones de muertes entre 1957 y 1958 y tuvo su origen en patos.
Puntos de origen de las pandemias modernas
En el caso poco probable de una pandemia causada por el H5N1, actualmente existen tres vacunas contra este virus que cuentan con la aprobación de la FDA. El gobierno de Canadá ha adquirido un suministro limitado de 500,000 dosis como medida preventiva ante un posible brote humano a gran escala. Por su parte, el gobierno del Reino Unido ha firmado un contrato para más de cinco millones de dosis de una vacuna contra la influenza H5 destinada a humanos.
Conclusión
Riesgo bajo, pero se requiere atención
El nivel de amenaza actual de una posible pandemia humana causada por el H5N1 puede clasificarse como “bajo”. Si bien existe motivo para mantener una vigilancia estrecha, la comunidad científica coincide, en términos generales, en que no hay razones para alarmarse por el momento.
Compartir esta información es clave para mantener y mejorar la salud pública. Mantenerse informado sobre la evolución del H5N1 es fundamental para evaluar los riesgos con precisión y adaptar las políticas de manera proactiva en un mundo cada vez más interconectado.
RGA participa activamente en la recopilación de datos de alta calidad y en el seguimiento riguroso de investigaciones de primer nivel. La compañía forma parte del comité ejecutivo del foro de liderazgo del Center for Infectious Disease Research and Policy (CIDRAP) de la Universidad de Minnesota, lo que le brinda acceso directo a los datos e información más recientes disponibles.
Colabora con RGA y accede al conocimiento más actualizado sobre riesgos de vida y salud. Conoce más hoy mismo.







