Durante más de 20 años, la ciencia médica ha visto una explosión de investigación productiva sobre la neuroinflamación (es decir, la respuesta inflamatoria que afecta al sistema nervioso).
Los investigadores también han estudiado el impacto de la neuroinflamación en muchas condiciones de salud adversas, incluidos trastornos neurodegenerativos como las demencias y la enfermedad de Parkinson, una variedad de condiciones psiquiátricas y estados de dolor persistente.
El nuevo conocimiento descarta creencias largamente sostenidas pero aparentemente incorrectas sobre la estructura y función del sistema nervioso y los procesos biológicos relacionados en el cuerpo humano.
La inflamación ha sido reconocida durante mucho tiempo como un proceso desencadenado por una lesión tisular o un asalto, con el propósito principal de defenderse y reparar después de la lesión o el asalto. Involucra una serie de acciones que incluyen funciones inmunológicas específicas de varios tipos de células, cada una con un conjunto diferente de funciones. Algunos tipos ingerirán y eliminarán sustancias que amenazan al individuo que experimenta la inflamación. Otros liberarán mediadores químicos, de los cuales hay muchos tipos diferentes con roles distintos pero a veces superpuestos.
Los procesos de la inflamación son integrales para la supervivencia del cuerpo. Se activan por infección o lesión y son de relevancia prominente en condiciones como enfermedades cardíacas, cáncer, diabetes y artritis. El papel de la inflamación en la sensibilización periférica y central en estados de dolor ha sido reconocido desde hace mucho tiempo. También se ha reconocido que, con diferentes modos, duraciones y circunstancias, la actividad inflamatoria y sus expresiones no siempre son beneficiosas y de hecho pueden volverse perjudiciales, como se tipifica, por ejemplo, en la enfermedad reumatológica.
Células gliales y neuroinflamación
Entre las creencias largamente mantenidas que ahora se están descartando están las relacionadas con las células gliales del sistema nervioso central (SNC). El sustantivo colectivo para este grupo de células se originó en la palabra griega para "pegamento" y se aplicó a una gama de células del SNC anteriormente consideradas esencialmente inactivas, cuyo único papel era proporcionar andamiaje para las neuronas, las células nerviosas activas del sistema nervioso. Un tipo de célula glial, el oligodendrocito, fue reconocido por proporcionar las muy importantes vainas de mielina alrededor de los axones de las células nerviosas de acción rápida, pero eso era todo.
En las últimas décadas, ha surgido un entendimiento de que las células gliales de hecho realizan una serie de funciones importantes relevantes para la neuroinflamación dentro del SNC (ver Tabla 1).
| Tabla 1: Tipos de Células Gliales, Sus Funciones e Implicaciones | ||
| Tipo de Célula | Rol en la Inflamación | Implicaciones en el Dolor |
| Microglia | • Responde a patógenos/lesiones – migra según sea necesario • Elimina células/desechos dañados • Libera citoquinas, quimiocinas, prostaglandinas, especies reactivas de oxígeno, ATP | Estimulada por la exposición repetida a opioides, provoca la liberación de mediadores inflamatorios que amplifican el dolor y distorsionan la señalización del dolor |
| Astrocitos | • Regula la liberación de neurotransmisores de las neuronas • Regula la barrera hematoencefálica • Promueve la actividad de los oligodendrocitos • Modera la formación de nuevas neuronas (neuroplasticidad) | Involucrada en respuesta al estrés neuronal o lesión, puede promover la destrucción nerviosa así como la reparación/reconstrucción nerviosa |
| Oligodendrocitos | Mielinización de axones – actividad dependiente | La actividad en la médula espinal implicada en la génesis y mantenimiento de estados de dolor crónico |
| Células Ependimarias | • Secretan y mantienen el fluido cerebroespinal • Limpieza de desechos | Aún no se conoce |
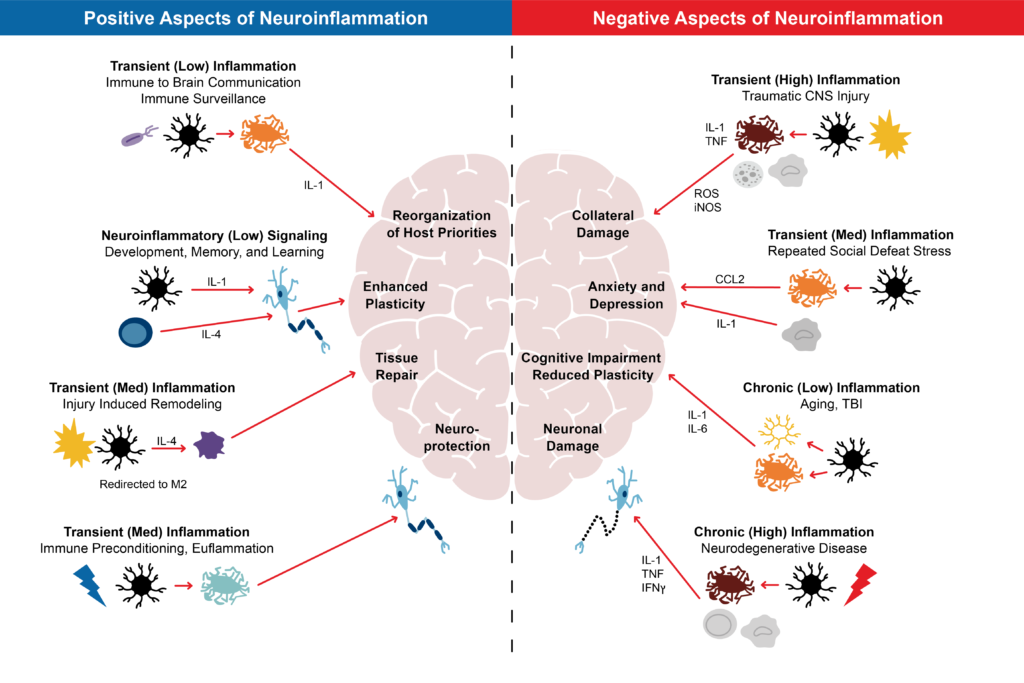
La respuesta inflamatoria no siempre es la misma dondequiera que ocurra. Variará según varios factores, incluida la naturaleza y el sitio de la lesión o agresión, su duración y elementos específicos del individuo. La neuroinflamación, por ejemplo, puede tener impactos positivos o negativos. Por un lado, puede estar asociada con la eliminación de elementos peligrosos y la reorganización de un sistema nervioso en reparación, pero por otro lado, puede estar relacionada con daños adicionales que pueden manifestarse de diversas formas. Además, se ha demostrado que la neuroplasticidad, un proceso importante en la recuperación de una lesión del SNC, puede ser tanto potenciada como reducida, dependiendo del tipo de actividad neuroinflamatoria.
Es notable que, si bien se ha detectado una actividad inflamatoria elevada en el SNC en casos de adversidad física, también se encuentra cuando hay amenaza emocional, y se ha demostrado que está asociada con estados de ánimo adversos como la ansiedad. Esta asociación biológica del estado de ánimo/ansiedad con la inflamación encontrada en condiciones como el dolor persistente puede ser una percepción importante para los pacientes y los profesionales que los cuidan y tratan.
Además de la actividad inflamatoria de las propias células gliales, los químicos mediadores que liberan causan el reclutamiento de células de respuesta inflamatoria desde el torrente sanguíneo. La actividad de estas últimas es facilitada por la permeabilidad alterada de la barrera hematoencefálica. Dicha barrera está compuesta por las células endoteliales que revisten todos los vasos sanguíneos así como, en el contexto del SNC, proyecciones de los astrocitos, las células gliales más abundantes. Son los astrocitos los que son principalmente responsables de la permeabilidad alterada de la barrera.
De hecho, las células gliales realizan una serie de funciones importantes relevantes para la neuroinflamación dentro del SNC.
La microglía, un tipo de célula glial, tiene dos roles: vigilancia inmune primaria e ingestión y eliminación de células no deseadas. Componiendo del 10% al 15% de las células en el SNC, la microglía proporciona roles neuroprotectores importantes y, como su renovación es lenta, son menos susceptibles a daños a largo plazo. Cuando se enfrentan a enfermedades y variando con el tipo de lesión o asalto, la microglía produce químicos inflamatorios que promueven el reclutamiento de otras células protectoras. Desafortunadamente, en ciertas situaciones, la actividad microglial puede volverse excesiva y/o persistente en detrimento del individuo. Tal actividad mejorada ha sido implicada en condiciones como estados de dolor persistente, condiciones neurodegenerativas y enfermedades mentales.
Las Conexiones de las Glías
Entrelazado con el conocimiento avanzado de la neuroinflamación está el papel de los factores dietéticos. La microbiota intestinal, término aplicado a los microorganismos que colonizan el tracto gastrointestinal, se sabe que cambia según una serie de variables, no siendo la menor de ellas los hábitos dietéticos de una persona.
La microbiota intestinal ahora es cada vez más reconocida como influyente fuera del tracto gastrointestinal. Esto incluye el SNC, con vínculos establecidos con la función cognitiva y las respuestas inmunitarias. Investigaciones han vinculado la disfunción microglial, causando neuroinflamación crónica y trastorno neurológico, con el desequilibrio del microbioma intestinal. El microbioma también ha sido encontrado impactando la actividad del eje hipotalámico-pituitario-adrenal (HPA), que está implicado en el desarrollo de trastornos neurológicos y psiquiátricos, así como de síndromes de fatiga.
También se postula un papel bidireccional para la comunicación entre el cerebro y el intestino para el nervio vago, y numerosos estudios señalan su influencia en la actividad neuroinflamatoria microglial.
Se sabe también que los químicos proinflamatorios son liberados por los excesivos depósitos de grasa llevados por individuos con sobrepeso, lo cual puede aumentar la percepción del dolor y las quejas.
Finalmente, y de manera importante, hay investigaciones emergentes sobre el papel de un hígado saludable en todos estos aspectos del dolor y su manejo, lo cual parece estar impactando estos sistemas. El eje hígado-cerebro es reconocido como influyente en procesos como el estrés oxidativo en el SNC y otros procesos metabólicos adversos involucrados con la neurodegeneración y la sensibilización central del procesamiento del dolor.
Los Vínculos con el Dolor
En relación con el dolor específicamente, se reconoce cada vez más que dos tipos de células gliales, los astrocitos y las microglías, desempeñan roles significativos en la aparición y persistencia de estados de dolor amplificado, el desorden de la neuro organización (como ocurre en la sensibilización central del dolor o el wind-up) y la reducción de la eficacia de los medicamentos opiáceos. La actividad de estas células implica la liberación de varios productos químicos inflamatorios, así como productos químicos moduladores y factores de crecimiento, que pueden llevar al desorden de las estructuras y redes neurales saludables dentro de la médula espinal y el cerebro. Aunque estos tipos celulares tienen poca o ninguna acción en situaciones normales de dolor, están involucrados en cambios que causan la amplificación del dolor a través de estas acciones inflamatorias. Desafortunadamente, su activación se ve aumentada por el uso persistente de opioides, y las propias células gliales muestran aumentos adicionales en la actividad en respuesta a la exposición crónica a los opioides. El impacto es la amplificación del dolor, la propagación del dolor más allá de su distribución original, cambios en el tipo e intensidad del dolor, y una reducción en la efectividad de los analgésicos opioides.
FIGURA 1: ASPECTOS DE LA NEUROINFLAMACIÓN
Implicaciones para el tratamiento
La conclusión más importante que se puede extraer de la investigación emergente es que los estados de dolor persistente no suelen ser un trastorno de la parte del cuerpo identificada como afectada. Aunque puede haber una patología continua del órgano o parte del cuerpo, también habrá un desorden dentro del sistema nervioso, particularmente en la médula espinal y el cerebro. Por esta razón, el dolor persistente debería considerarse quizás como una enfermedad o condición por derecho propio, más allá de la parte del cuerpo afectada identificada.6
Hay muchos factores impulsores que contribuyen al dolor persistente, y todos deben ser reconocidos y abordados.
Los intentos de tratar el dolor con estrategias que se centran únicamente en la lesión o enfermedad inicial están fallando en reconocer y abordar la patología del sistema nervioso que puede surgir, y que puede aumentar y perpetuar la angustia y disfunción del paciente.
La investigación continúa profundizando en enfoques biológicos para manipular los mecanismos citados en este artículo. Algunos son menos específicos, como la estimulación del nervio vago, mientras que otros son intentos más enfocados de manipular la actividad de los químicos inflamatorios de acción central liberados por las células gliales y otras células implicadas. Esto ha estimulado el interés en la posibilidad de aprovechar estos mecanismos con agentes anestésicos e incluso antibióticos, pero hasta ahora no se han logrado avances terapéuticos sólidos.
El mensaje para los pacientes con dolor persistente y sus cuidadores médicos es que hay muchos factores impulsores que contribuyen al dolor persistente, y todos deben ser reconocidos y abordados. Como se indica, estos incluyen un énfasis excesivo en tratar la fuente presunta del dolor, el uso continuo de medicamentos opiáceos y la falta de atención a los factores psicológicos asociados con el estrés. Idealmente, esta investigación emergente debería explicarse al paciente con el fin de promover la comprensión del dolor persistente como un estado de enfermedad tanto del sistema nervioso completo como de la persona completa. Esa comprensión también debería usarse para alentar la adopción clínica de un enfoque "de toda la persona" para mejorar la propensión del cuerpo y del cerebro a la inflamación mientras se revierte la tendencia al deterioro general.