Han pasado 60 años desde que se lanzó la icónica película "Los Pájaros" de Alfred Hitchcock, basada en los verdaderos eventos de un ataque masivo de aves en California. Hoy, el virus de la influenza A aviar ha creado su propio drama.
Los informes de infecciones humanas han sido esporádicos, pero la circulación del virus de la influenza aviar altamente patógena (HPAI) ha ido en aumento en especies aviares y mamíferos como zorros rojos, focas y visones.
Afortunadamente, las tasas de infección por influenza aviar en humanos siguen siendo bajas y están principalmente confinadas a aquellos que han estado en contacto directo con aves enfermas o muertas que albergan la enfermedad. De hecho, la propagación ha llevado al sacrificio masivo de aves de corral. La preocupación no es el número de infecciones humanas reportadas, sino el potencial del virus de la influenza aviar (AIV) para mutar aún más, permitiendo la transmisión de humano a humano y el inicio de otra pandemia.
¿Qué es el Virus de la Influenza Aviar (VIA)?
Existen cuatro tipos de virus de la influenza; A, B, C y D. VIA, apodado 'gripe aviar', es un virus tipo A altamente contagioso que se propaga entre aves acuáticas silvestres, causando una grave enfermedad respiratoria. Inicialmente confinado a Asia, el tipo A ha aparecido en África, Europa y América del Norte y recientemente se ha extendido hacia el sur desde México hasta el sur de Chile. Los mamíferos que se alimentan de aves silvestres también se están infectando, lo que resultó en un evento masivo de mortalidad de 3,487 lobos marinos sudamericanos en Perú a principios de 2023. (1)
Subtipos
El VIA tiene muchos subtipos basados en dos proteínas, hemaglutinina (HA) y neuraminidasa (NA). Por ejemplo, el virus H5N1 tiene una proteína HA 5 y una proteína NA 1.(2) Las modificaciones virales pueden ocurrir por deriva antigénica, donde surgen pequeñas mutaciones debido a la influencia del huésped, o por cambio antigénico, donde ocurre una reasignación genética para crear nuevos subtipos de HA o NA, dejando a un huésped humano sin ninguna defensa inmunológica contra la nueva cepa del virus debido a la falta de exposición previa. (3)
H5N1, H5N6, H5N8, H6N1, H7N2, H7N3, H7N7, H7N9, H9N2, H10N7 y H10N8 son conocidos por infectar a humanos. Mientras que síntomas leves que están asociados con los subtipos H6N1, H7N2, H7N3 y H7N7, H5N1 y H7N9 pueden causar síntomas graves en humanos, llevando a una alta tasa de mortalidad. (3) Las cepas virales que provienen de huéspedes animales con nuevos subtipos de HA o NA son las más propensas a impactar el riesgo de pandemia. Estas nuevas cepas pueden propagarse rápidamente a través de la población humana debido a la falta de inmunidad. (4)
El clado actual (el virus original y sus descendientes) del virus H5N1 es conocido como 2.3.4.4b. Se han informado casos de H5N1 2.3.4.4b desde Chile, China, Inglaterra, Ecuador, España y EE. UU., con una letalidad reportada en China. La infección AIV H5 más reciente fue identificada en dos trabajadores avícolas en Inglaterra en mayo de 2023. Es importante destacar que no se ha informado transmisión de humano a humano en ninguno de estos casos.
H7N9 es un VIA potencialmente pandémico ya que es común en los mercados de aves, puede superar las barreras del huésped, no existen anticuerpos neutralizantes preexistentes, tiene una reasignación genética con H9N2 y se adapta a un huésped humano. H5N1 y H7N9 son de mayor preocupación debido a sus altas tasas de mortalidad.(7) El Centro para el Control y la Prevención de Enfermedades (CDC) de EE. UU. actualmente clasifica el riesgo pandémico del virus H5N1 clado 2.3.4.4b como moderado y H7N9 como moderado-alto. (8)
Síntomas y Tratamientos
La enfermedad humana puede ocurrir tras el contacto con heces de aves infectadas, saliva o alimentos y agua contaminados; por lo tanto, los trabajadores avícolas tienen un mayor riesgo de infección que la población general. El inicio de los síntomas tras la infección inicial suele aparecer después de tres a cinco días. Para la infección por H5N1, la incubación en humanos es entre dos y cinco días, pero puede ser de hasta 17 días. (3) Los síntomas de la gripe aviar incluyen dolor de cabeza, dolores musculares, tos o falta de aliento y fiebre muy alta. Otros síntomas pueden incluir diarrea, náuseas, dolor en el pecho, conjuntivitis y hemorragia nasal.(7) En casos graves, puede llevar a encefalitis, neumonía, fallo multiorgánico y síndrome de dificultad respiratoria aguda (SDRA), ya que los pulmones de los afectados experimentan destrucción alveolar difusa y sangrado. Cargas virales altas, linfopenia y niveles elevados de citocinas han sido asociados con resultados fatales en individuos infectados con H5N1.(3)
Los tratamientos incluyen medicamentos antivirales como Tamiflu (oseltamivir), Rabivab (peramivir) y Relenza (zanamivir), que tienen como objetivo reducir la gravedad de los síntomas, prevenir complicaciones y mejorar las posibilidades de supervivencia. Todos los medicamentos son inhibidores de NA y son más efectivos cuando se toman temprano en las infecciones. Sin embargo, la mejor defensa contra el virus de la influenza sigue siendo la vacunación.(7)
Historia de la infección humana por influenza aviar
En 1918, el subtipo H1N1 causó la pandemia de la Gripe Española, resultando en millones de muertes en todo el mundo. Esto fue seguido por la pandemia de la Gripe Asiática en 1957 (H2N2), la pandemia de la Gripe China en 1968 (H3N2) y la pandemia global de 'gripe porcina' H1N1 en 2009.(3) El H5N1 es actualmente la cepa más problemática del virus de la gripe. Identificado por primera vez en 1959, permaneció sin detectar hasta 1996 cuando el virus fue encontrado en gansos en el sur de China y Hong Kong. En 1997, 18 personas se infectaron con H5N1 resultando en seis muertes; el virus no volvió a surgir en humanos hasta 2003.(9) La cepa altamente patógena H7N9 fue identificada por primera vez en humanos en China en 2013, y el país experimentó varias oleadas de infección hasta 2017. Los casos identificados fuera de China se encontraron en personas que habían viajado desde el país.(4)
Tasas de infección y mortalidad
Durante la grave pandemia de 1918, más de 500 millones de personas (aproximadamente un tercio de la población mundial de ese momento) se infectaron con H1N1, y entre cincuenta y cien millones de personas se informó que habían muerto. Se informó que la pandemia de H3N2 de 1968 mató al 0.03% de la población mundial, pero para la pandemia de H1N1 de 2009, solo del 0.001% al 0.007% de la población mundial murió durante los primeros 12 meses. Aun así, esto representó entre 700 millones y 1.4 mil millones de infecciones humanas y entre 151,700 y 575,400 muertes, una tasa de mortalidad entre el 0.02% y 0.04%.(3, 10)
Los subtipos AIV H5N1 y H7N9 son los de mayor preocupación ya que pueden causar síntomas graves en humanos, llevando a una alta tasa de mortalidad. A nivel mundial, hasta el 2 de junio de 2023, ha habido 876 infecciones humanas con H5N1, incluyendo 458 muertes informadas en 23 países desde 2004, una tasa de mortalidad del 52.2%, mientras que H7N9 ha causado 1,567 infecciones humanas y 615 muertes, una tasa de mortalidad del 39%. (4, 6)
FIGURA 1: DISTRIBUCIÓN DE CASOS HUMANOS CONFIRMADOS DE INFECCIÓN POR H5N1 POR AÑO DE INICIO Y PAÍS (2003-2023)(6)
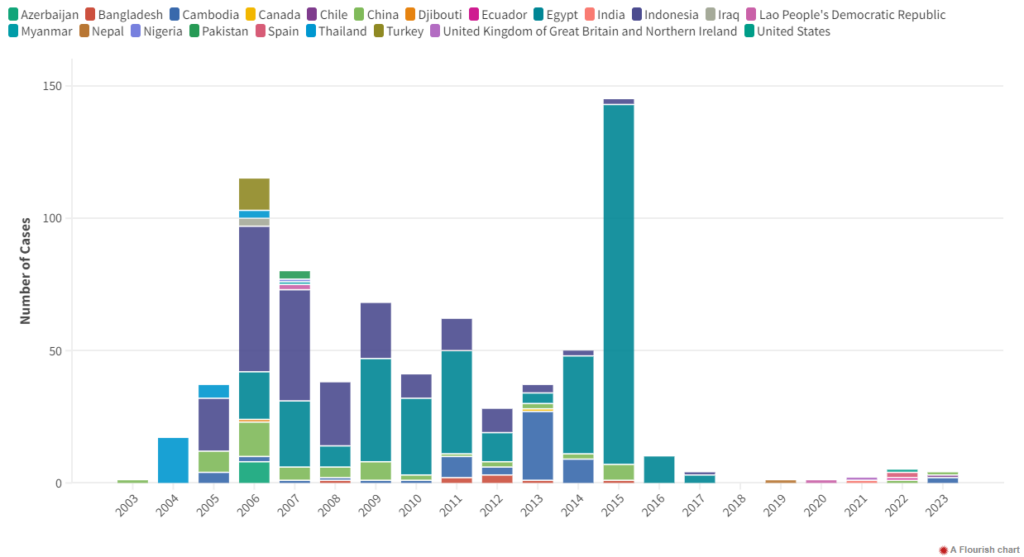
*Nota: Incluye dos detecciones informadas en 2022 desde España y una de Estados Unidos debido a la sospecha de contaminación ambiental y sin evidencia de infección.
H5N6 ha sido reportado en China y Laos, causando 84 infecciones humanas y 29 muertes posteriores, una tasa de mortalidad del 35%.(1) H9N2, identificado por primera vez en humanos en 1998, es un AIV de baja patogenicidad y, por lo tanto, difiere en virulencia de H5N1 y H7N9. Como no es una infección notificable, solo se han registrado 124 infecciones humanas y una muerte.(6)
Desde la pandemia de "gripe porcina" de 2009, el virus de la influenza A H1N1 circula estacionalmente, causando múltiples infecciones, hospitalizaciones y muertes. El CDC estima que en los EE. UU., desde 2009 hasta 2018 hubo más de 100 millones de infecciones, de las cuales menos del 1% de los individuos fueron hospitalizados. Se informaron 75,000 muertes, una tasa de mortalidad del 0.075%. (11)
Vacunas
Una de las formas de combatir una pandemia es a través de la inmunidad masiva de la población. La inmunidad puede ocurrir ya sea por infección natural o vacunación. La creación de vacunas es un proceso largo y arduo, pero como ya existen vacunas contra la influenza aprobadas, adaptarlas a nuevas cepas generalmente lleva alrededor de 6 meses.(4)
El desarrollo de las vacunas de ácido ribonucleico mensajero (ARNm) no es nuevo, pero cobraron protagonismo durante la pandemia de COVID-19 cuando se aprobaron rápidamente en respuesta al brote viral de SARS-CoV-2 en humanos. Las vacunas de ARNm tienen muchas ventajas, especialmente como parte de una respuesta pandémica, ya que se pueden fabricar rápidamente y son altamente escalables.
En 2016, la Agencia Europea de Medicamentos (EMA) otorgó la aprobación de comercialización condicional para la vacuna contra la influenza pandémica H5N1 de AstraZeneca, lo que significa que fue aprobada en interés de la salud pública basándose en datos menos exhaustivos de lo normalmente requerido, ya que el medicamento abordaba una necesidad médica no satisfecha.(12) La Administración de Alimentos y Medicamentos (FDA) de los EE. UU. también ha autorizado el uso de dos vacunas contra el virus de la influenza H5N1.(13)
Vigilancia
En 1982, la OMS estableció una red global de vigilancia de la influenza, conocida como el Sistema Global de Vigilancia y Respuesta a la Influenza (GISRS). Se creó para preparar, monitorear, alertar y responder a brotes de influenza. Posteriormente, desarrolló la 'Herramienta de Evaluación del Riesgo de Pandemia de Influenza' (TIPRA) en 2016 para estimar el riesgo de una pandemia por nuevas cepas de influenza.1
El CDC también tiene una herramienta de evaluación del riesgo de pandemia potencial presentada por los virus de la influenza A, conocida como la Herramienta de Evaluación del Riesgo de Influenza (IRAT).(8) Ambos modelos de la OMS y del CDC toman en consideración características como la transmisión viral en modelos animales, la inmunidad de la población, la gravedad de la enfermedad, las tasas de infección en humanos y animales, la composición genómica del virus y la propagación geográfica de la enfermedad en la evaluación de riesgos.
FIGURA 2: PUNTUACIONES DE RIESGO DE EMERGENCIA E IMPACTO DEL VIRUS IRAT DEL CDC (VER TABLA PARA MÁS DETALLES)(8)
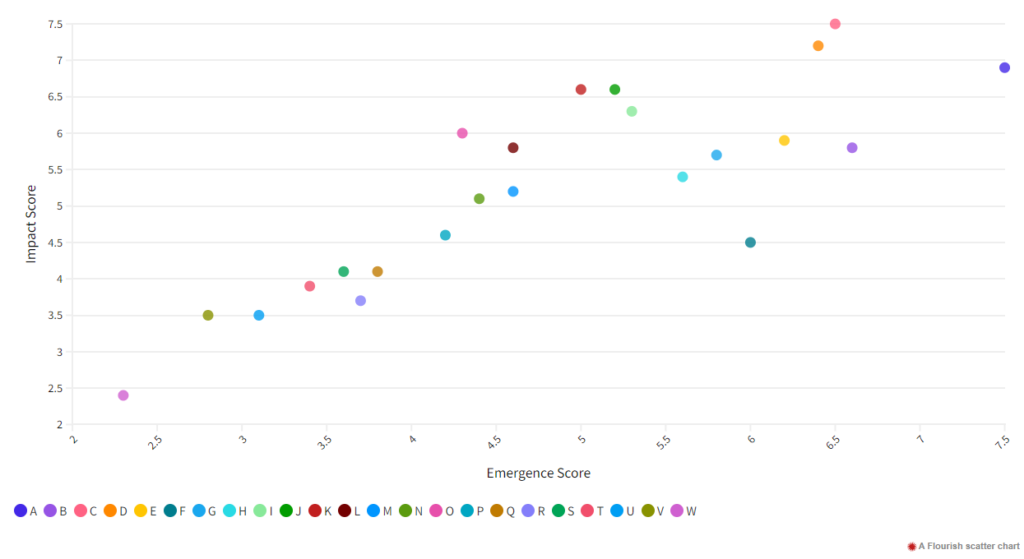
Conclusiones
Con el virus de la influenza aviar circulando ahora entre múltiples especies animales, hay una mayor probabilidad de que el AIV mute y se vuelva más infeccioso en humanos. En la actualidad, las infecciones humanas con AIV tienden a ser el resultado directo del manejo de aves infectadas y no debido a la transmisión de humano a humano. Sin embargo, el AIV tiene potencial de pandemia debido a la aparición de nuevos subtipos virales, incluidos H5N1 y H7N9, ambos con una alta tasa de mortalidad. A medida que el virus continúa propagándose en aves y animales, se pueden esperar más infecciones humanas. Como aún no se ha adaptado para permitir una transmisión sostenida de humano a humano, la probabilidad de una pandemia de influenza aviar es actualmente muy baja.












